Санирование и восстановление влажных и
засоленных фасадов
1.
Что мы наблюдаем?
Красивые
фасады современных кирпичных зданий щедро украшены беспорядочными белыми
разводами. Они появляются достаточно быстро после возведения дома,
озадачивая строителей и хозяев. Предпринимаются активные действия по
устранению белых пятен и потеков - некрасиво! В ход идут доморощенные
средства: моют водой и соляной кислотой, мажут соляркой и растительным
маслом, покрывают цветной краской и лаком. Результат один – пятна на
поверхности появляются снова, покрытия отслаиваются местами, и снять их
полностью без повреждения кирпича практически не удается.
2.
Что это за пятна?
Белесый
вид новенького красного кирпича вызывает недоумение. Первое, что
приходит в голову – это остатки кладочного раствора, небрежно
оставленные строителями. Вторая мысль – работали зимой и не пожалели в
раствор соли. Но потеки не группируются вокруг швов, они рассеяны
совершенно произвольно. Ответ приходит только в результате анализа. В
случае строительного раствора или популярной противоморозной добавки –
поташа водный раствор должен иметь щелочную среду, однако, в абсолютном
большинстве случаев анализ соскобов демонстрирует среду, близкую к
нейтральной.
Качественный анализ анионов в этих случаях дает
положительную реакцию на сульфат-ион, причем соль, как правило,
полностью растворяется в холодной воде, что исключено для такого
сульфата как гипс. Реже и слабее проявляется хлорид-ион. Вывод
напрашивается один – в составе высола присутствуют чаще всего
водорастворимые сульфаты, самым распространенным из которых является
сульфат натрия.
3.
Откуда
эти соли?
Применяемый в качестве антифриза поташ встречается в кладочных швах и
порой в немалых количествах. Серый раствор становится грязно-белым, а
если шов закрашен краской, то белые потеки прорываются и через краску.
Произвольная дозировка солей, будь то поташ или поваренная соль,
обязательно даст результат – не связанные соли выйдут наружу, навстречу
влаге. Водорастворимые хлориды натрия и кальция встречаются на нижней
части фасадов, омываемых талыми водами, в которых велика концентрация
этих солей – антиобледенителей. Нитраты (селитры) попадают в грунтовые
воды от смыва дождями избытка сельскохозяйственных удобрений, из
фекальных вод, а также в результате действия на почву кислых атмосферных
осадков, содержащих оксиды азота из выбросов промышленных предприятий и
ТЭЦ.
Чаще всего и в больших количествах встречаются
сульфаты и, прежде всего, сульфат натрия. Характерно то, что
концентрации сульфатов в современном кирпиче по причинам техногенного
характера значительно выше, чем в кирпиче старинных построек. Это может
быть связано с источниками поступления сернистых соединений, как со
стороны почвы, так и со стороны атмосферы. Загрязнение карьеров
сульфатами обусловлено накоплением в почве продуктов разложения
поверхностно-активных моющих веществ – сульфонатов натрия, поступающих с
коммунальными сточными водами. Микроорганизмы почв, разлагая сульфонат,
перерабатывают органическую часть молекулы, оставляя в грунтах
минеральный сульфат. С другой стороны атмосфера принимает большое
количество сернистого газа от перерабатываемого дизельного топлива и из
выбросов промышленных предприятий. Кислые сернистые дожди способствуют
накапливанию в почвах сульфатов щелочных металлов и прежде всего,
сульфата натрия, наиболее распространенного в земной коре щелочного
металла. Водорастворимые сульфаты калия и магния встречаются в грунтах
значительно реже, в основном вблизи морских акваторий и магнезитовых
жил.
4.
Чем
опасны эти соли для строительного сооружения?
Попадая в
кирпич из сырьевой глиняной массы в процессе изготовления изделий или из
грунтовых и талых вод при эксплуатации здания, соли постепенно начинают
свою разрушительную работу.
Капиллярно-пористая структура строительных
материалов, обусловленная их природой, структурой, условиями получения,
физической (капиллярной) усадкой, а также причинами естественного и
техногенного старения, способствует интенсивной миграции влаги в стенах
сооружения. Глинистые грунты, способствующие высокому уровню залегания
грунтовых вод, скопления талых и дождевых вод, отсутствие эффективных
дренажных и гидроизоляционных систем создают условия для капиллярного
движения грунтовых и атмосферных вод. Реально мигрирует уже не вода, а
солевой раствор, охватывающий значительные участки стен.
Испаряя
воду, раствор оставляет на поверхности солевые разводы, называемые
высолами. Непривлекательный вид фасада – только малая часть тех
факторов, которые могут нанести сооружению непоправимый вред. Рассмотрим
основные моменты солевой агрессии.
4.1 Гигроскопичность солей
Соли
магния, кальция и натрия имеют малые размеры катионных радиусов – табл.
1, поэтому легко притягивают значительные количества диполей воды.
Хлориды магния и кальция термодинамически
устойчивы в виде кристаллогидратов переменной структуры, а сульфат
натрия – в виде десятиводного кристаллогидрата
Na2SO4.10H2O.
1.
MgCl2*nH2O (n
– переменная величина )
2.
MgSO4*nН2О
--- “ ---
3.
CaCl2*nH2O (n
– переменная величина )
4.
Na2CO3*nН2О --- “ ---
5.
Na2SO4*10Н2О – устойчивый кристаллогидрат
Таблица 1.
Радиусы
катионов
|
Катион
|
Радиус иона,
Å |
|
Mg2+ |
0,61 |
|
Са2+ |
1,02 |
|
Na+ |
0,95 |
|
K+ |
1,33 |
В зависимости от температуры и уровня влажности
среды в теле кирпича и на его поверхности с той или иной скоростью
начинают идти попеременные процессы испарения воды и кристаллизации
солей в виде твердых кристаллогидратов – объемных гидрофильных
образований.
|
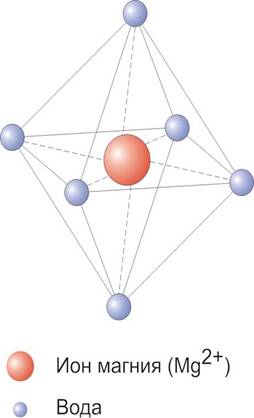
Сульфат
магния |
Сульфат натрия |
|
 |
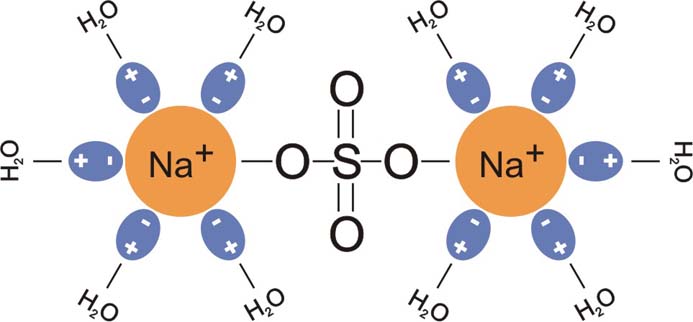 |
На схемах
указаны: шестиводный сульфат магния, где ион магния образует устойчивый
октаэдрический кристаллогидрат, теряющий воду лишь при 200оС,
и десятиводный кристаллогидрат сульфата натрия – плоская форма, теряет
воду при 32оС.
Гигроскопические свойства солей способствуют усиленному поглощению
стенами влаги из воздуха, и даже в отсутствие капиллярного подсоса
грунтовых вод и непосредственных атмосферных осадков провоцируют
отсыревание кладки. При отрицательных температурах замерзание воды
приводит к увеличению объема. Давление льда разрушает тонкие
межкапиллярные стенки, способствуя расширению и разветвлению поровой
структуры кирпича.
4.2 Создаваемое солями давление и его периодичность
Учитывая возможность процессов гидратации солей,
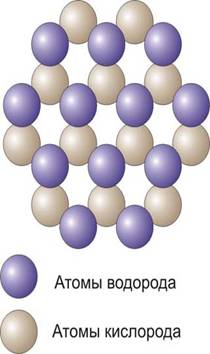
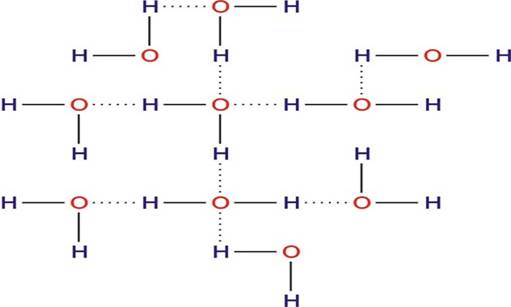
следует иметь в виду тот факт, что вода имеет полимерный характер.
Ассоциаты полимерных форм в состоянии льда состоят из 5 молекул, а при
переходе в жидкую фазу могут включать до 10 и более единичных молекул.
Вода с учетом ее молекулярной массы (18) имеет аномально высокие
значения плотности и температуры кипения, существенно превышающие
аналогичные показатели у соединений с большими значениями молекулярных
масс, например, у бензола и его производных с молекулярными массами
около 100, низших спиртов (этанол) и т.п. Данную аномалию можно
объяснить только спецификой молекулярной структуры.
|
Лёд |
Вода |
|
 |
 |
|
|
|
|
По
указанным причинам масса и соответственно объем кристаллогидратов на
порядок и более могут превышать массу и объем безводной соли.
При насыщении кирпича влагой соли могут вновь
растворяться и затем кристаллизоваться повторно. Кроме того,
кристаллогидраты при температурах более 30оС могут терять
кристаллизационную воду полностью или частично (табл.2), вновь
присоединяя ее в вечернее время с уходом солнца и повышением влажности.
Таблица 2
Потеря
солями гидратационной воды
|
MgSO4*7H2O |
150oC |
MgSO4*6H2O |
200oC |
MgSO4*1H2O |
|
Na2SO4*10Н2О |
32,4oC |
Na2SO4 |
|
|
|
Ca(NO3)2*4H2O |
30oC |
Ca(NO3)2*3H2O |
100oC |
Ca(NO3)2 |
Таблица
наглядно иллюстрирует характерную особенность десятиводного сульфата
натрия, полностью терять воду при температуре выше 32оС а
затем стремительно ее набирать при понижении температуры и повышении
влажности воздуха.
Возникающее периодически кристаллизационное и
гидратационное давление (табл.3), а также увеличение объема солевой
массы за счет гидратации неизбежно приводят к явлениям отшелушивания,
трещинообразования и постепенной деструкции кирпича. Если кирпич покрыт
цементно-песчаной штукатуркой, возможны трещины и локальные отслоения.
Таблица3
Давление
кристаллизации и гидратации сульфата натрия
|
Соль |
Давление кристаллизации, МПа |
Давление гидратации, МПа |
|
Na2SO4*10Н2О |
7,2 (0OC);
8,3 (50оС) |
98,2 (0оС)*;
67,4 (20оС)* |
|
Na2SO4 |
29,2
(0оС); 34,5 (50оС) |
|
* - при 100% относительной влажности воздуха
Выход солей
на поверхность фасадов – процесс неизбежный, поскольку соли мигрируют
навстречу влаге, стремясь к образованию своей энергетически устойчивой
модификации – кристаллогидрату. Будучи водорастворимыми, они вымываются
атмосферными осадками, освобождая место новым порциям солей, которые,
вымываясь в свою очередь, способствуют многократному развитию сети
капилляров и пор. Увеличивающееся водопоглощение создает серьезную
угрозу замораживания-размораживания и соответственно – разрушения
кирпичной массы
5.
Как очистить и защитить засоленный фасад?
Удалить водорастворимые соли систематической водоструйной обработкой
стен не представляется возможным, ибо процесс выхода солей на
поверхность носит перманентный характер. Сильное увлажнение кирпичной
кладки нежелательно.
Как
очистить
кирпич
в
этом
случае?
Ни
в
коем
случае
нельзя
прибегать
к
советам
случайных
людей:
например
мыть
фасад
соляной
кислотой.
Соляная
кислота
разрушает
кладочный
раствор,
сильно
открывает
поры
кирпича,
и
миграция
солей
на
поверхность
лишь
усиливается,
при
этом вносится дополнительное количество хлор-ионов.
Оптимальный вариант - перевести соли на поверхности в труднорастворимую
форму действием так называемых флюатов – солей кремнефтористоводородной
кислоты. Тем самым крупные поверхностные поры окажутся заблокированными
для транспорта водорастворимых солей из тела кирпича на поверхность, и
перспектива кристаллизационного давления на отделочный слой существенно
снижается.
После
механической очистки стен от выступивших труднорастворимых образований
рекомендуется оштукатуривание фасада пористыми известково-цементными
растворами. Цементно-песчаные штукатурки плохо пропускают пар, который,
конденсируясь на границе раздела, может привести к намоканию несущих
стен.
Применение гидрофобных, пористых, трещиностойких штукатурок создает
реальную возможность долговечной защиты фасада. Такие штукатурки
называются санирующими или осушающими. Приготовленные на легких
заполнителях (вспученные минеральные и органические материалы –
керамзит, перлит, полистирол) и содержащие специальные добавки
известково-цементные штукатурки содержат до 30% воздушных
гидрофобизованных пор. Они не принимают на себя функций несущих
конструкций и не деформируются при осадке дома. Такие штукатурки
обладают способностью «дышать», т.е. пропускать пары воды без
конденсации на границе раздела, равномерно распределяют частично
мигрирующие соли в порах, не давая им скапливаться в разделительном слое
и срывать покрытие. Гидрофобизованные поры защищают штукатурку от
внешнего воздействия влаги и воды.
Санирующие штукатурки признаны в настоящее время лучшей защитой от влаги
при наличии в кладке гидрофильных (гигроскопических) солей. В данных
условиях без специальных франкирующих мероприятий (флюатирование) не
спасает применение отсечной горизонтальной или вертикальной
гидроизоляции.
Если
оставить кирпичный фасад в натуральном виде, без оштукатуривания,
следует избавиться от солей и предпринять соответствующие меры:
а)
очистить фасад разбавленным раствором кислотного очистителя на базе
органической кислоты, который удалит остатки строительного раствора,
растворимые и труднорастворимые соли и освободит поры поверхности;
б)
обработать фасад гидрофобизирующей жидкостью. Как правило, это
кремнийорганические композиции в виде растворов или водных дисперсий.
Активная часть композиции отверждается под действием углекислого газа
воздуха, выстилая стенки капилляров и пор защитной водонепроницаемой, но
паропроницаемой пленкой. Чем меньше воды в составе пропиточного
раствора, тем быстрее идет процесс отверждения. Наиболее эффективными
гидрофобизаторами являются кремнийорганические жидкости силоксанового
типа на органических растворителях. Такие жидкости быстро обеспечивают
водоотталкивающий эффект. В результате гидрофобизации капли воды
скатываются с фасада, не впитываясь в материал, а глубинные соли не
имеют возможности выхода на поверхность. Кирпич защищен от
кристаллизации и гидратации солей, от процессов
замораживания-размораживания, а, следовательно, и от разрушения.
6.
Как
защитить фасад от грунтовых вод?
Защита
строительных сооружений от проникновения воды предполагает разные
способы поверхностной и объемной гидроизоляции и гидрофобизации. Если
речь идет о поверхностной защите, то в основе лежит физическое
взаимодействие с несущей конструкцией, где решающую роль играют вопросы
адгезии или степени пропитки жидкостью пористых материалов. Химические
реакции твердения жидких фаз или дисперсий осуществляются затем под
действием внутренних причин или внешнего (атмосферного) воздействия.
Объемная (отсечная) гидроизоляция – один из
наиболее эффективных способов защиты от грунтовой влаги – основана на
химических процессах, имеющих место либо в условиях атмосферных, либо за
счет реакций с составляющими строительного материала. Во втором случае
чрезвычайно важно знать, возможны ли химические реакции с компонентами
материала в данном конкретном сооружении. Реакционноспособной
составляющей известковой или цементной композиции является гидроксид
кальция – свободная известь. Поэтому действие агентов объемной
гидроизолирующей системы направлено именно на реакцию с известью с целью
связывания ее в труднорастворимые кальциевые гидросиликаты,
закупоривающие капилляры или сужающие их диаметр (2,3):
</BLOCKQ< td>
Более подробную информацию получите по телефону
8-926-535-39-36 |